
Non esiste una tecnica standard per la chirurgia laser endovenosa dell’insufficienza venosa cronica. Si può parlare più correttamente di “best practice”, cioè di una buona prassi basata sulla pratica clinica e sulle evidenze scientifiche, riassunte nelle linee guida.
Discutere la “best practice” della tecnica ELVeS richiede di scomporre la procedura nelle sue fasi successive:
1. mappatura preoperatoria ecografica
2. gestione dell’ambiente operatorio
3. anestesia (tumescenza)
4. operatività pratica della procedura endovenosa e gestione post-operatoria del paziente.
La gestione dell’ambiente operatorio è essenziale per la buona riuscita dell’intervento, sia in termini di temperatura e luminosità sia in termini di corretto atteggiamento dell’operatore e del personale di sala.
È importante comunicare con il paziente, avere un’attitudine alla pazienza, alla gentilezza e alla comprensione dell’ansia di chi sta per affrontare un intervento endovenoso senza la protezione psicologica dell’anestesia generale.
Occorre quindi dedicare il giusto tempo all’esecuzione dell’anestesia locale per tumescenza, sfruttandone appieno, oltre all’azione analgesica, gli altri suoi vantaggi:
• dissociare i tessuti e le strutture perivasali
• garantire un adeguato isolamento termico del vaso.
Una tumescenza condotta correttamente è importante inoltre per ottenere migliori risultati estetici, per esempio per limitare il rischio di iperpigmentazioni, di solito temporanee ma talora anche definitive, o di teleangectasie reattive in caso di safene soprafasciali.
Come ampiamente dimostrato da Giorgio Spreafico, un’adeguata anestesia per tumescenza può essere realizzata con 20 cc. di lidocaina 2%, 5 cc. di bicarbonato di sodio e 2 cc 2 cc. di una soluzione di adrenalina ottenuta diluendo 1 mg di adrenalina in 10 cc di fisiologica, per 500 ml di soluzione fisiologica (J Vasc Surg Venous Lymphat Disord 2014; 2:403-10). La concentrazione finale di lidocaina nella solu- zione è pari allo 0,076%, sufficiente per ottenere l’azione analgesica evitando gli effetti indesiderati dell’anestetico.
L’anestesia per tumescenza deve essere praticata sotto guida ecografica, procedendo in direzione cranio-caudale dalla crosse verso il tronco safenico e dal piano profondo al piano superficiale.
Con il paziente in posizione anti-Trendelemburg, s’inizia con la puntura percutanea della safena sotto controllo ecografico; la guida e l’introduttore 6F sono posizionati sotto controllo visivo. Sempre con controllo ecografico e guidati dalla luce pilota, viene poi inserita la fibra laser fino a livello della giunzione.
Il controllo ecografico è indispensabile per il posizionamento finale della fibra, sia in proiezione trasversale che longitudinale. Si procede distalmente al “punto di atterraggio” e quindi si retrae lentamente la fibra sino a circa 2 cm dalla giunzione.
Una volta posizionato il paziente in Trendelemburg, si effettua un controllo ecografico finale della posizione della fibra, si posiziona un repere sulla fibra a ridosso dell’introduttore e si procede alla tumescenza.
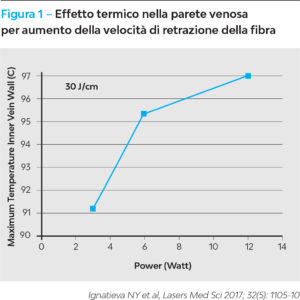
La termoablazione è condotta in modo continuo. La potenza impiegata varia da 7 a 10 W per la grande safena ed è di 5 W per la piccola safena. L’energia erogata in joule/cm varia in funzione del diametro della vena, moltiplicato x 20 per il trattamento della crosse e x 10 per il trattamento del tronco. Per diametri alla crosse > 1 cm, occorre ricordare che un maggior effetto termico si ottiene aumentando la potenza (W) e la velocità di retrazione (cm/sec), mantenendo costante la LEED (densità di energia endovenosa lineare), (Figura 1).
La procedura si conclude con la rimozione della fibra, il controllo visivo della sua integrità e con il controllo finale ecografico della pervietà del sistema venoso profondo. Recentemente, in letteratura emergono robuste evidenze circa i risultati a breve, medio e lungo termine relativi alle tecniche termoablative.
In particolare, Aurshina et al. riportano una percentuale di ricanalizzazione dell’ 8.8% nei pazienti sottoposti a trattamento laser rispetto al 10% nei pazienti sottoposti a radiofrequenza, ad un follow-up medio di 13.5 mesi (p = 0.54) (Ann Vasc Surg 2018;52:158-162).
Lo studio Varico 2 ha confermato tali risultati anche ad un follow-up di 5 anni (Lawson et al. J Vasc Surg Venous
Lymphat Disord 2018;6:31-40).
Le linee guida della Società Europea di Chirurgia Vascolare (ESVS) riassumono le indicazioni emerse dagli studi descritti, descrivendo le tecniche di ablazione termica endovenosa come prima scelta per il trattamento del reflusso safenico (Wittens C, Davies AH. Eur J Endovasc Surg 2015;49:678-737).
In conclusione, il laser endovenoso si dimostra una tecnica efficace, basata sulla pratica clinica e su una robusta evidenza scientifica. La metodica è riproducibile e sicura, con l’ulteriore beneficio di una breve curva di apprendimento.
 Home
Home


